当研究室は2013年に立ち上がったばかりの新しい研究室ですが、ヒトiPS細胞の作製技術、維持培養、分化誘導技術、人工がん幹細胞作製技術などを駆使して、がんを中心とした疾患の診断・治療への貢献をめざした研究をおこなっています。現在は、主に下記の4つのテーマに取り組んでいます。
1. 人工がん幹細胞を用いたがん幹細胞の特性解析とがん治療への応用
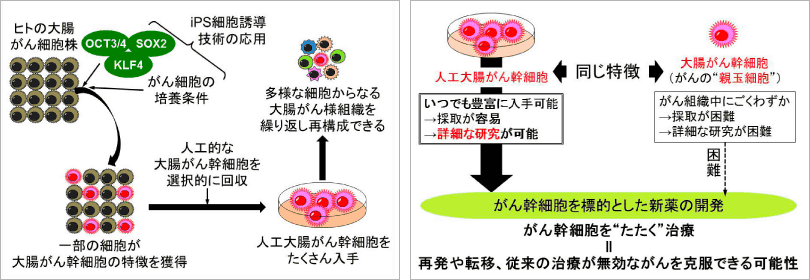
ヒトのがん細胞は様々な細胞から構成されるヘテロな集団であり、このことが、がんの治療を難しくしているとされています。その中でも、がん幹細胞といわれる一部の細胞群は自己複製能、抗がん剤抵抗能、スフェア形成能、腫瘍形成能、多様性形成能を持ち、がんの再発転移、治療抵抗性の原因とされ、新規治療標的として注目されています。しかしながら、このがん幹細胞はがん組織中にほんのわずかにしか存在せず、またがん組織の入手自体も手術が行われる機関やタイミングの制約を受けることから、その起源や特性獲得の分子機構の解析が困難でした。そのような中で我々は2014年、大腸がんの細胞株に3つの因子(OCT3/4, SOX2, KLF4)を導入することでがん幹細胞の特性をもった細胞、すなわち人工大腸がん幹細胞を作製し、これを選択的に回収することに成功しました。
(Oshima et al., 2014, PMID: 25006808)
本手法はがん幹細胞研究に用いるサンプルの量的および時機的制約を解消するもので、がん幹細胞の特性の獲得や維持に係る分子機構の解明を通じて、がん幹細胞を標的とした診断、治療法の開発に役立つことが期待されています。現在は大腸がん以外のがんもターゲットとし、より純度の高い人工がん幹細胞の培養維持方法や特性解析を進めています。
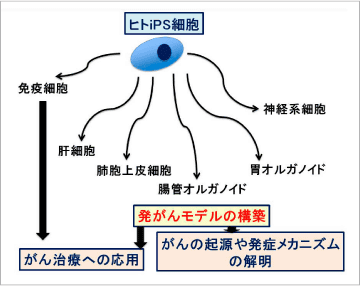
2. ヒトiPS細胞からの分化細胞を用いた発がんモデルの構築とがん治療への応用
体細胞からiPS細胞を作成する技術については、近年ほぼ統一された手法が確立されてきましたが、iPS細胞から様々な細胞を作成する技術については、目的とする細胞ごとに完成度も異なる上に、まだ課題も多く、世界中で多くの研究者が取り組んでいるところです。我々の研究室では、ヒトiPS細胞を様々な細胞へと分化誘導するプロトコールの最適化に取り組んでいます。こうして得られた細胞にがんの原因となる候補遺伝子を導入するなどして各種発がんモデルを構築し、がんの発症メカニズムの解析や治療へ応用することを目的とした研究を行っています。また、ヒトiPS細胞を用いるがん免疫療法の開発にも取り組んでいます。
3. 人工がん幹細胞やヒトiPS細胞からの分化誘導系を用いたヒト内在性
レトロウイルスの新規機能の探索
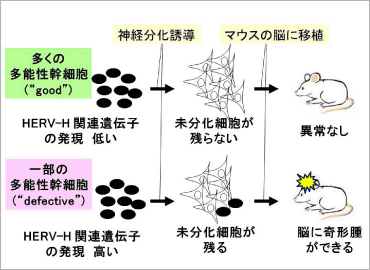
ヒト内在性レトロウイルス(human endogenous retrovirus、以下HERV)は太古の昔に我々の祖先のゲノムDNAに取り込まれました。その多くは進化の過程で変異や欠失を繰り返し、不活性化されていると言われています。我々は、一部のヒトiPS細胞でこのHERVの一種(HERV-H)に関連する遺伝子が活性化し、そのことが神経細胞への分化を阻害し、移植後の奇形腫形成に関与することを見つけました (Koyanagi-Aoi & Ohnuki et al., 2013、PMID:24259714)。このHERV-Hは、一部のがん細胞においても活性化していることが報告されていますが、活性化の具体的なメカニズムやその意義はわかっていません。我々は、このHERVが、がんを含む疾患とどのように関連しているのか(HERVの悪い側面)、あるいは生体の維持にどのように関連しているのか(HERVの良い側面)について、人工がん幹細胞やヒトiPS細胞からの様々な分化誘導系を用いて研究し、これまで知られていなかったHERVの機能を明らかにしていきたいと考えています。
4. 疾患特異的iPS細胞の作製と病態再現、創薬への応用
神戸大学内の各診療科との共同研究により、疾患特異的iPS細胞を作製し、肝、消化管、神経、皮膚、内分泌など様々な細胞への分化誘導を行って、病態の再現、創薬への応用を視野にいれた研究を行っています。